1 引言
黑索金(RDX)是一种常用的烈性炸药。目前,行业内常采用液相色谱法定量测定RDX的含量,但该法需要用到RDX的标准物质,在无标准物质的情况下无法进行定量检测。原子发射检测器(AED)是气相色谱(GC)的一种元素型检测器,能进行多元素检测的同时还具有元素的等摩尔效应[1-5],其元素信号的响应值与元素的绝对质量相关而与元素所在的化合物结构无关[6-8],因此GC-AED能够通过非自身标样定量测定包含相同元素的化合物[9-15]。
本文中采用GC-AED对RDX进行非自身标样的定量检测新方法研究,首先通过元素谱线的灵敏度实验确定最佳定量元素谱线,再通过定量响应因子选择最佳外标物,然后采用外标法,基于外标物的元素标准曲线对RDX进行定量测定,建立了一种RDX的非自身标样定量分析方法。
2 实验部分
2.1 仪器与试剂
安捷伦7890A气相色谱仪(美国安捷伦科技公司);JAS AED微波诱导原子发射光谱检测器(德国JAS公司);电子分析天平(瑞士梅特勒-托利多公司);HP-5毛细管柱(30 m×0.32 mm×0.25 μm,美国安捷伦公司);容量瓶(100 mL,1 L);丙酮(分析纯,四川西陇化工有限公司);DBP(分析纯,国药集团化学试剂有限公司);DBS(分析纯,国药集团化学试剂有限公司);乙酰苯胺(纯度标准品,Sigma-Aldrich贸易有限公司);苯甲酸(纯度标准品,中国计量科学研究院提供);RDX、二苯胺纯度标准品由西安近代化学研究所提供。
2.2 仪器工作条件
GC参数:进样口温度200 ℃;柱温170 ℃;载气为高纯氦气(99.99%);恒流模式,柱流量3 mL/min;分流比20∶1;进样体积0.5 μL。
AED参数:实验中用到的元素谱线分别为C(193 nm)、C(496 nm)和N(174 nm);反应气:C(193 nm)和N(174 nm)使用的反应气为H2和O2,C(496 nm)使用的反应气为O2;检测器腔体温度250 ℃;检测器传输线温度220 ℃;数据采集频率为50 Hz。
2.3 标准曲线溶液配制
用电子分析天平准确称取RDX 2.02 g、苯甲酸1.62 g、乙酰苯胺1.70 g、二苯胺1.74 g、邻苯二甲酸二丁酯(DBP)样品2.06 g、癸二酸二丁酯(DBS)样品2.12 g(以上样品精确至0.01 g),分别放入1 L容量瓶中,用丙酮定容至刻度,作为标准使用液。将4种样品的标准使用液分别取100、50、25、6.3、3.1 mL置于100 mL容量瓶中,用丙酮定容至刻度,完成标准曲线溶液的配制。
3 结果与讨论
3.1 元素谱线初筛
RDX含有C、H、O、N 4种元素,其中,H元素的含量较少,O元素使用的反应气含有CH4,容易使检测器产生积碳而影响元素的响应信号,所以用这2种元素定量待测物易引起较大误差。C、N元素的常用元素谱线有C(193 nm)、C(496 nm)、C(179 nm)、N(388 nm)和N(174 nm)等,其中,N(388 nm)的反应气有CH4,C(179 nm)的元素信号强度较弱,所以一般情况下这2条元素谱线并不常用于定量检测。因此通过初筛,本研究选择C(193 nm)、C(496 nm)和N(174 nm)进行灵敏度实验,再根据灵敏度实验结果选择定量元素谱线。
3.2 定量元素谱线选择
用电子天平称取RDX 0.14 g(精确至0.01 g),放入 100 mL容量瓶中,用丙酮定容至刻度。将配制好的RDX标准品溶液按照选定的仪器工作条件下进样,通过C(193 nm)、C(496 nm)和N(174 nm)3条元素谱线平行测定3次,得到单位浓度(μg/mL)的元素峰面积响应值,计算其平均值(S平均),结果见表1。
表1 灵敏度实验结果
Table 1 Experimental results of sensitivity

样品元素谱线S平均RDXC(193 nm)68.33C(496 nm)0.13N(174 nm)1.09
由表1可知C(193 nm)、C(496 nm)和N(174 nm)单位浓度的元素峰面积响应值分别为68.33、0.13和1.09,所以在相同的实验条件下,不同元素谱线具有不同的元素峰面积响应值。相比较而言,C(193 nm)单位浓度的元素峰面积响应值较大,具有较高的灵敏度,为最佳灵敏线。因此,本研究选择C(193 nm)作为定量元素谱线。
3.3 外标物选择
将RDX、苯甲酸、乙酰苯胺、二苯胺、DBP、DBS的标准曲线溶液在选定的仪器工作条件下分别进样,以C(193 nm)为定量元素谱线,平行测定6次,记录不同浓度下对应C元素峰面积及其平均值。本研究以测得C元素峰面积(y)的平均值和质量浓度(x,μg/mL)绘制标准曲线,测得6种样品的C元素标准曲线的函数表达式如表2。
标准曲线斜率即为单位浓度的C元素峰面积响应值,本研究将标准曲线斜率作为样品的绝对定量响应因子。由表2可知,6种样品的绝对定量响应因子各不相同,说明元素的等摩尔效应可能与样品的理化性质、化学结构、实验条件等因素有一定关系,具体原因还有待进一步研究。通过比较可知,随着保留时间的增加,不同样品的绝对定量响应因子逐渐减小,保留时间越接近,绝对定量响应因子的误差越小。因此在进行外标物的选择时,可以优先考虑与待测物保留时间相近的化合物,再结合标准曲线,找出峰面积响应值与待测物相近的化合物作外标物进行定量检测。
表2 元素标准曲线函数表达式测定结果
Table 2 Determination results of element standard curves
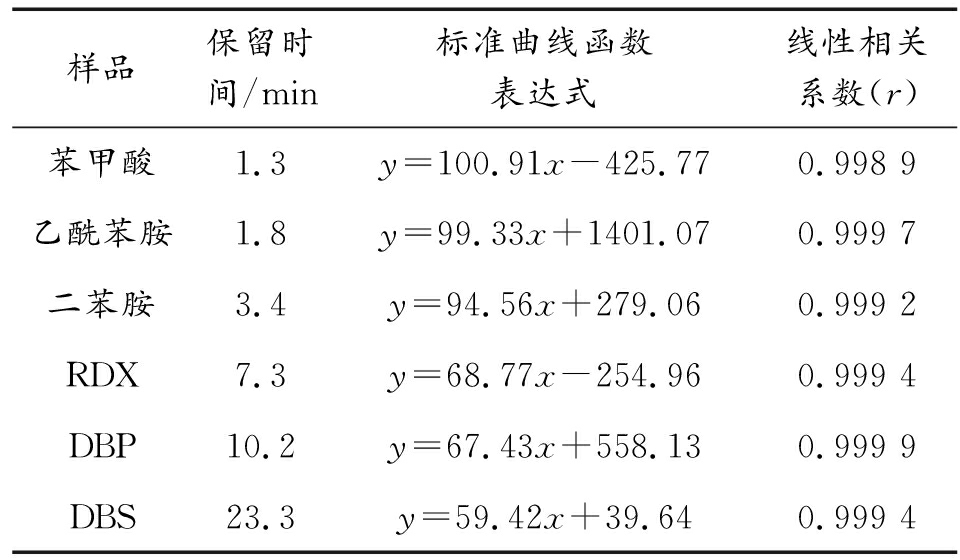
样品保留时间/min标准曲线函数表达式线性相关系数(r)苯甲酸1.3y=100.91x-425.770.998 9乙酰苯胺1.8y=99.33x+1401.070.999 7二苯胺3.4y=94.56x+279.060.999 2RDX7.3y=68.77x-254.960.999 4DBP10.2y=67.43x+558.130.999 9DBS23.3y=59.42x+39.640.999 4
通过比对6种样品的绝对定量响应因子,可知RDX和DBP的绝对定量响应因子仅相差1.34,说明RDX和DBP有非常相近的C元素峰面积响应值。并且RDX和DBP的C元素标准曲线的相关系数(r)分别为0.999 4和0.999 9,线性关系良好,因此DBP为最佳外标物。以DBP为外标物,通过DBP的C元素标准曲线能够定量测定RDX的C元素浓度,再结合分子式即可得到RDX的含量。
在选定的色谱条件下,该方法定量测定RDX的浓度线性范围为0.07~2.02 mg/mL。以3倍信噪比计算检测限,测得RDX的方法检测限为0.06 μg/mL。
3.4 精密度和准确度评价
本研究用加标回收率评价方法的准确度,用相对标准偏差(RSD)评价方法的精密度。配制线性范围内高、中、低浓度的RDX标准溶液,在选定的仪器工作条件下平行测定6次,记录不同浓度下对应C元素峰面积及其平均值,计算加标回收率和相对标准偏差(RSD),结果见表3。
表3 精密度和准确度实验结果
Table 3 Experimental results of precision and accuracy
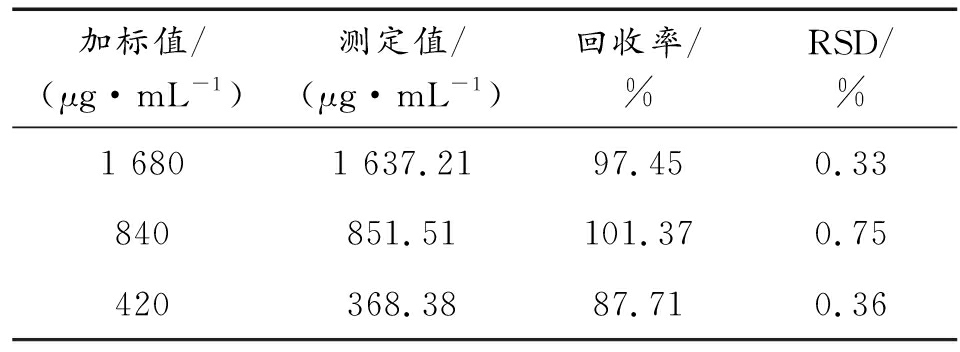
加标值/(μg·mL-1)测定值/(μg·mL-1)回收率/%RSD/%1 6801 637.2197.450.33840851.51101.370.75420368.3887.710.36
由表3可知,RDX在线性范围内高、中、低浓度的相对标准偏差(RSD)分别为0.33%、0.75%和0.36%,线形范围内高、中、低浓度的加标回收率分别为97.45%、101.37%和87.71%。结果表明,线性范围内中高段的回收率较好,而低段浓度由于浓度值接近线性范围的边缘,容易引起误差,致使准确度较差,所以进行定量分析时应避免配制线形范围内的低段浓度,确保定量结果的准确度。
3.5 验证实验
用电子天平称取0.6 g含RDX的某含能样品,将其置于烧杯中,加入60 mL丙酮使其完全溶解,经过滤、稀释完成RDX样品溶液的配制。
液相色谱法(LC法)是定量测定RDX的一种常规方法,为了验证GC-AED法的可行性,本研究分别通过GC-AED法和LC法进行RDX的含量测定,平行测定6次。将获得的两组数据首先进行F检验,分析GC-AED法和LC法测定结果的方差有无显著性差异,以此来比较两种方法的精密度;再进行t检验,分析两组数据的平均值有无显著性差异,以此来比较2种方法的准确度。GC-AED色谱分离曲线如图1所示,6次平行测定的结果如表4。
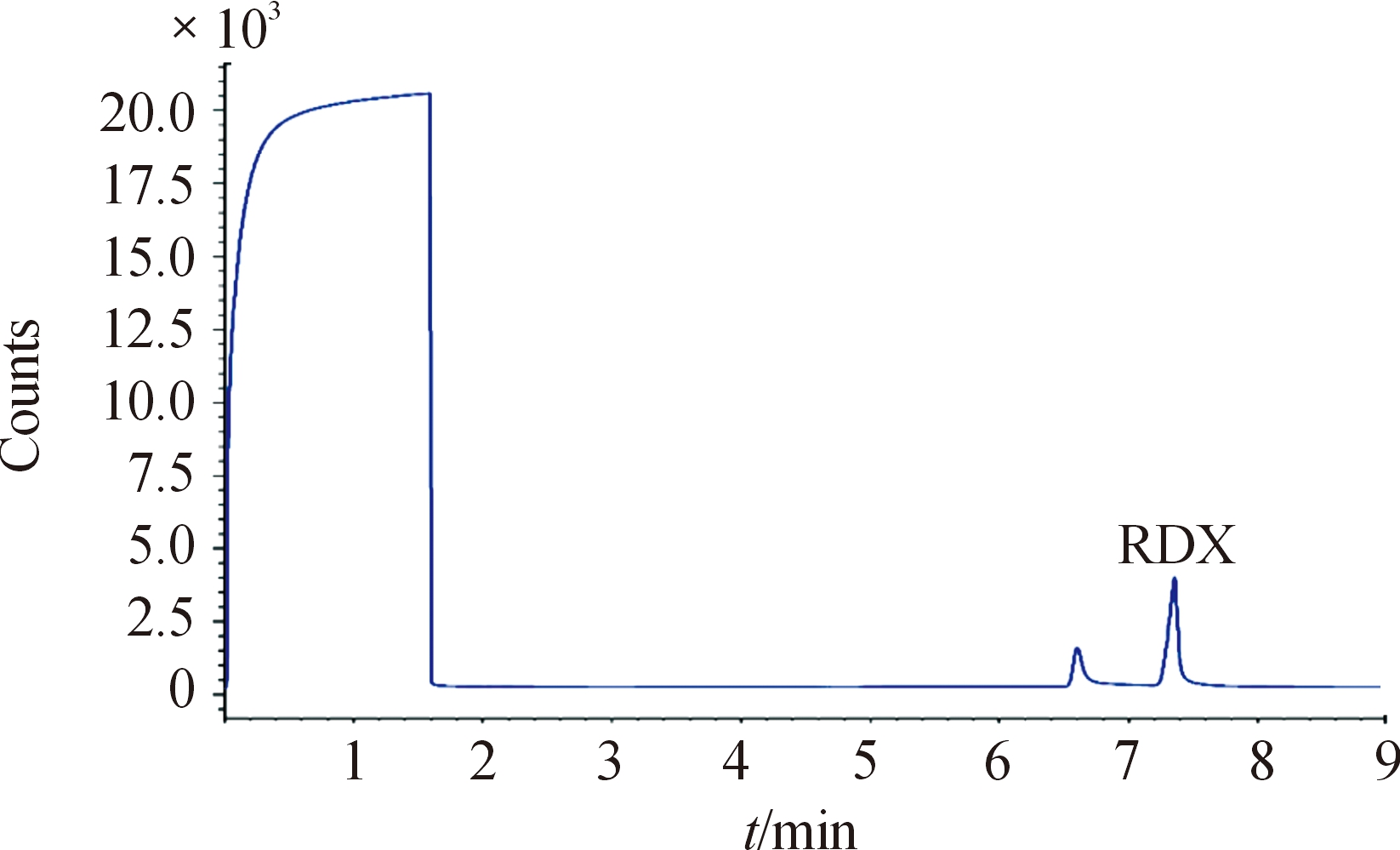
图1 GC-AED色谱分离曲线
Fig.1 Chromatographic separation diagram of GC-AED
表4 实际样品测定结果(质量分数,%)
Table 4 Determination results of actual samples
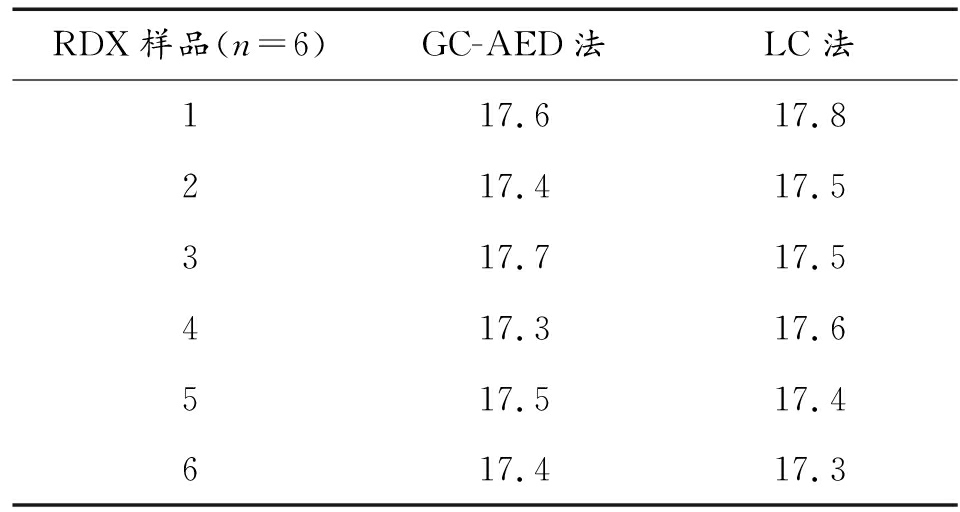
RDX样品(n=6)GC-AED法LC法117.617.8217.417.5317.717.5417.317.6517.517.4617.417.3
通过F检验计算得到的F计算值为1.37,查F分布表可知,当置信因子为0.05,样本量为6时,得到F表为5.05,因为5.05>1.37,所以2组数据的方差没有显著性差异,进而能够判断GC-AED法和LC法测定结果的精密度没有显著性差异。通过t检验计算得到的t计算值为0.36,查t分布表可知,当置信因子为0.05,样本量为6时,得到t表为2.23,因为2.23>0.36,所以2组数据的平均值没有显著性差异,进而能够判断GC-AED法和LC法测定结果的准确度没有显著性差异。以上实验结果证明采用GC-AED法定量分析RDX的组分含量是可行的。
4 结论
1) 采用气相色谱-原子发射检测器(GC-AED)建立了RDX的非自身标样定量分析新方法,该方法以C(193 nm)为定量元素谱线,以 DBP为外标物,基于DBP的C(193 nm)元素标准曲线定量测定RDX的C元素含量,再结合分子式得到RDX的含量。
2) 该方法能够通过非自身标样对RDX进行定量分析,灵敏度高,具有较好的准确度和精密度,有效解决了无RDX标准物质带来的定量检测难题。
[1] 辛仁轩.等离子体发射光谱分析[M].北京:化学工业出版社,2005.
Xin R X.Analysis of plasma emission spectra[M].Beijing:Chemical Industry Press,2005.
[2] 赵贵喜,梁冰,杨永坛.等离子体原子发射光谱检测器在气相色谱中的应用进展[J].现代科学仪器,2005(2):30-34.
Zhao G X,Liang B,Yang Y T.Application of plasma atomic emission spectral detectors in gas chromatography[J].Modern Scientific Instrument,2005(2):30-34.
[3] 周永新,李前远,靳志云,等.用气相色谱-原子发射光谱法检测VX、Bz及其降解产物[J].分析测试学报,2000,19(3):79-81.
Zhou Y X,Li Q Y,Jin Z Y,et al.VX、Bz and its degradation products detected by gas chromatography-atomic emission spectrometry[J].Journal of Analytical Testing,2000,19(3):79-81.
[4] Toshimitsu O,Morio K,Yoshitaka I,et al.Aplication of solid-phase extraction to the analysis of the isomers generated in biodesulfurization against methylated dibenzothiophenes[J].Journal of Chromatography A,2000,903(1/2):193-202.
[5] Natalia C,Rosa P,Nerea A,et al.Solid-phase microextraction andgas chromatography with atomic emission detection for multiresidue determination of pesticides in honey[J].Analytica Chimica Acta,2006,562(1):9-15.
[6] 袁懋,师宇华,于爱民,等.用于气相色谱的微波等离子体原子发射光谱检测器的发展[J].色谱,2007,25(3):310-315.
Yuan M,Shi Y H,Yu A M,et al.Development of microwave plasma atomic emission spectral detectors for gas chromatography[J].Chromatography,2007,25(3):310-315.
[7] 王清清,顾明松.气相色谱-微波诱导等离子体原子发射光谱的应用进展[J].分析化学,2004,32(8):1093-1098.
Wang Q Q,Gu M S.Application progress of gas chromatography-microwave induced plasma emission spectra[J].Analytical Chemistry,2004,32(8):1093-1098.
[8] Taegon K,Jaewook R,Min J K,et al.Characterization and analysis of vanadium and nickel species in atmosphericresidues[J].Fuel,2014(117):783-791.
[9] 靳志云,顾明松,罗毅.气相色谱-原子发射光谱联用仪对安眠镇静类和局麻类药物的非同一标样定量分析[J].药学学报,1997,32(11):865-868.
Jin Z Y,Gu M S,Luo Y.Quantitative analysis of non-identical standard samples of sleeping and sedative drugs and local anesthetics by gas chromatography-atomic emission spectra[J].Journal of Pharmacy,1997,32(11):865-868.
[10] 宋婷婷,陈佳,郭磊,等.染毒全血与尿样中痕量路易氏剂的气相色谱-原子发射光谱联用法检测[J].分析测试学报,2008,27(8):800-803.
Song T T,Chen J,Guo L,et al.Detection of Trace Lewy Agent in Poisoned Whole Blood and UrineSamples by Gas Chromatography-Atomic Emission Spectrometry[J].Journal of Analytical Testing,2008,27(8):800-803.
[11] 罗茜,马立新,夏传海,等.气相色谱/质谱与气相色谱/原子发射光谱联用分析多氯邻羟基二苯醚类化合物[J].分析化学,2004,32(7):852-856.
Luo Q,Ma L X,Xia C H,et al.Analysis of polychlorinated O-hydroxydiphenyl ether compounds by gas chromatography/mass spectra and gas chromatography/atomic emission spectra[J].Analytical Chemistry,2004,32(7):852-856.
[12] Yang Y T,Yang H Y,Zong B N,et al.Gas Chromatography-Atomic Emission Spectra Analysis Method and Application of Sulfide in FCC Gasoline[J].Analytical Chemistry,2003,31(10):1153-1158.
[13] Tsuyoshi K,Hiroaki Y,Shinichi S.The determination by gas chromatography with atomic emission detection of total sulfur in fuels used as forensic evidence[J].Forensic Science International,2008,177(2/3):112-119.
[14] Pan R R,Qu G L,Ma G H,et al.CIC Method of GC-AED for Quantitative Determination of Neurotoxic Agents[J].Chemical Engineer,2007(2):36-37.
[15] Natalia C,Rosa P,Manuel H C.Solid-phase microextraction for the determination of haloanisoles in wines and other alcoholic beverages using gas chromatography and atomic emission detection[J].Journal of ChromatographyA,2008,1210(2):222-228.